Kimia: Asas/Atom
Dalam Bahasa Melayu, kita kadang kala akan berjumpa dengan perkataan zarah. Zarah adalah perkataan Bahasa Arab yang membawa maksud "habuk yang halus sekali". Ia juga membawa maksud "bahagian kecil sesuatu jirim". Bahagian kecil inilah yang disebut sebagai atom.
Apa itu atom?
[sunting]Atom adalah bahagian terkecil sesuatu jirim. Semua benda yang berada di sekeliling kita terdiri daripada atom. Saiz sebuah atom adalah jauh lebih kecil daripada mana-mana hidupan di Bumi.
Kimia mengkaji interaksi antara atom-atom: bagaimana sifatnya secara tunggal dan bagaimana ia bergabung dan berpisah antara atom-atom lain. Sesetengah atom boleh bergabung dengan mudah dengan atom lain, dan sesetengah yang lain tidak boleh bertindak balas langsung dengan mana-mana atom. Ada atom yang boleh mengalirkan cas elektrik, ada yang tidak. Jarak antara atom berbeza mengikut fasa sesuatu jirimnya. Kelakuan sesuatu atom menentukan kelakuan sesuatu jirim.
Bahagian-bahagian atom
[sunting]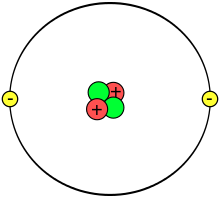
| Zarah | Jisim (kg) | Jisim relatif | Cas |
|---|---|---|---|
| Proton | 1.67 × 10-27 | 1840 | + |
| Neutron | 1.67 × 10-27 | 1840 | 0 |
| Elektron | 9.11 × 10-31 | 1 | - |
Rajah 3.1 Gambar rajah ringkas atom helium-4.
Atom terdiri daripada tiga zarah iaitu proton, neutron dan elektron. Zarah-zarah ini membentuk dua bahagian atom ini, nukleus atom dan petala-petala elektron di sekelilingnya.
Proton (p+) ialah salah satu daripada dua zarah yang membentuk nukleus sebuah atom. Proton memiliki cas positif dan memegang elektron pada orbitnya. Jumlah proton yang terdapat dalam sebuah atom menentukan nombor atom, dan oleh itu unsur atom itu.
Neutron (n0) ialah satu lagi zarah yang membentuk nukleus atom. Neutron mempunyai berat yang sama dengan proton, tetapi ia tidak memiliki sebarang cas (dengan erti kata lain, ia bercas neutral). Jumlah neutron dalam satu atom menentukan isotop sesuatu atom. Setiap atom mempunyai neutron kecuali atom hidrogen-1 yang hanya mempunyai 1 proton di nukleusnya.
Bersama-sama, proton dan neutron dipanggil nukleon, iaitu zarah yang membentuk nukleus.
Elektron (e-) pula adalah zarah yang mengelilingi nukleus atom. Ia merupakan zarah terkecil dalam sistem ini dengan berat 1/1840 daripada berat nukleon, dan ia membawa cas negatif. Dalam satu atom neutral (bukan ion), jumlah elektron di sekeliling atom adalah sama dengan jumlah proton di nukleus. Tidak seperti proton dan neutron, elektron boleh keluar masuk atom dengan mudah, dan perubahan dalam jumlah elektron menentukan cas sebuah atom. Elektron adalah bahagian atom yang terlibat dalam pengikatan kimia dan penghasilan sebatian-sebatian kimia.
Elektron-elektron mengelilingi nukleus atom pada jarak tertentu yang tetap, dan laluan ini dikenali sebagai petala elektron (electron shell). Ia boleh terus mengelilingi nukleus kerana ia mempunyai tenaganya sendiri yang mengelakkannya terus jatuh ke nukleus, sama seperi Bulan yang tidak jatuh ke Bumi kerana ia mempunyai tenaga kinetiknya sendiri. Tenaga ini juga mengekalkan laluan elektron dan mengelakkannya daripada berubah.
Sejarah teori atom
[sunting]Teori atom telah bermula sejak zaman Yunani purba lagi. Konsep atomisme dan kewujudan atom telah dicadangkan oleh Democritus, seorang ahli falsafah Yunani. Beliau menganggap bahawa semua benda dibentuk oleh atom yang tidak boleh dimusnahkan dan terdapat dalam pelbagai bentuk. Atom-atom ini bergerak dalam satu "ruang kosong" dan kadang kala berhimpun dengan atom lain untuk membentuk sekumpulan atom yang menjadi sebatian.
Model atom pertama telah dicadangkan oleh John Dalton pada tahun 1805-1808. Beliau mengatakan bahawa atom terdiri daripada zarah-zarah sfera sangat kecil yang tidak boleh dibahagi yang dipanggil atom. Atom-atom unsur yang sama adalah serupa dan ia bergabung dengan atom yang lain dalam nisbah nombor bulat. Beliau juga menjelaskan bahawa atom tidak diciptakan dan tidak dimusnahkan, dan dalam satu tindak balas kimia, atom-atom hanya dipindahkan daripada satu bahan ke bahan yang lain. "Hukum keringkasan terhebat" yang berkait dengan model atomnya menimbulkan kontroversi dan ia akhirnya digantikan lebih kurang seabad kemudian.
Pada tahun 1897, J.J. Thomson telah menemui elektron. Berdasarkan penemuan ini, beliau telah mencadangkan model atom yang baru pada tahun 1904, iaitu model plum-pudding. Thomson mengatakan bahawa atom terdiri daripada satu sfera bercas positif ("pudding") dan di dalamnya terdapat elektron-elektron bercas negatif ("plum").
